Digital Therapeutics
코로나19로 디지털치료제 수요 ↑…美 FDA, 올해만 6개 허가
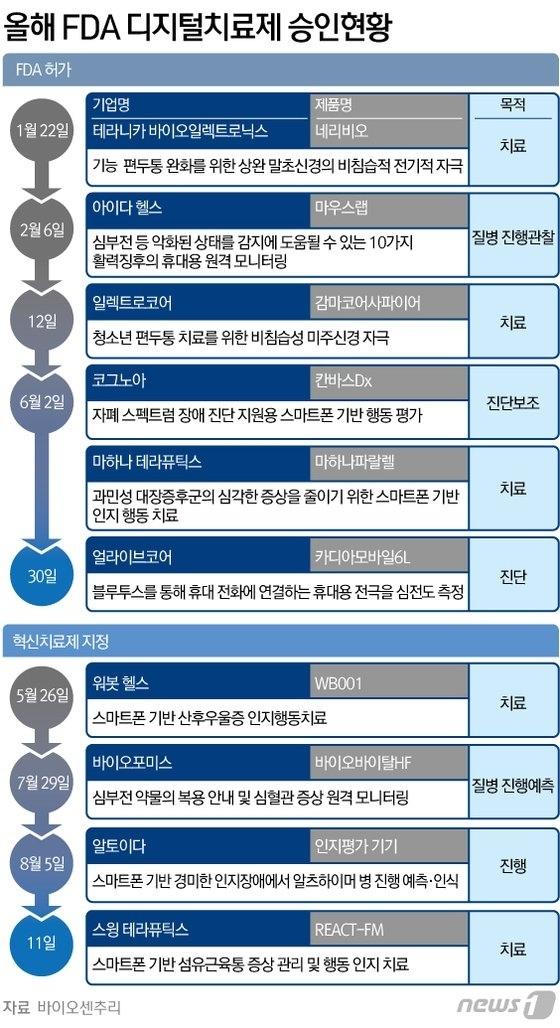
올해 들어 미국 식품의약국(FDA)으로부터 허가를 받은 디지털치료제가 6개인 것으로 나타났다. 혁신 치료제로 지정받은 후보도 4개에 이른다. 최근 신종 코로나바이러스 감염증(코로나19)으로 병원 방문이 줄어들면서 디지털치료제에 대한 수요가 꾸준하게 늘어나고 있는 것으로 보인다.
미국 바이오센추리는 25일(현지시간) 이같이 밝히며 질병의 원격 진단, 모니터링 또는 치료를 돕는 이 디지털 도구들의 의료분야 진출이 늘어나고 있다고 설명했다.
디지털치료제는 소프트웨어 프로그램을 통해 질병의 치료 및 예방 또는 관리할 수 있는 도구다. 스마트폰 애플리케이션, 게임, 인공지능 등을 이용해 환자들을 치료할 수 있다. 보통의 건강관리 제품과 달리 환자들의 생태를 개선하는 '치료제'인 만큼 임상시험을 통해 규제기관의 허가를 받아야 한다.
바이오센추리에 따르면 FDA는 지난 2014년부터 소수의 디지털치료제에 대한 품목허가를 승인하고 있다.
바이오센추리는 몸에 착용 가능한 웨어러블 센서와 디지털 애플리케이션은 실제 환자들의 상태와 치료 경과에 대해 실시간으로 지속적인 관찰이 가능해 환자들의 치료를 혁신적으로 개선할 수 있다고 설명했다.
올해 FDA로부터 허가를 받은 제품 중 2개는 이미 이전에 다른 형태 또는 다른 환자들을 대상으로 한번 허가를 받았던 제품이다. 일렉트로코어의 편두통 디지털치료제 '감마코어 사파이어(gammaCore
Sapphire)'는 지난 2018년 FDA로부터 허가를 받았으나 지난 2월 청소년을 대상으로 적응 대상을 확대했다.
얼라이브코어의 개인용 심전도 장치인 '카디아모바일
6L(KardiaMobile 6L)' 또한 2019년 처음 FDA 허가를 획득했다. 얼라이브코어는 환자들 맥박의 QTc 간격 계산을 할 수 있도록 개선해 지난 6월 추가로 승인받았다.
바이오센추리는 이밖에도 FDA로부터 승인이나 혁신치료제로 지정된 후 투자유치에 성공한 기업들도 있다고 설명했다.
마하나테라퓨틱스(Mahana
Therapeutics)는 FDA로부터 과민성대장증후군을 적응증으로 한 디지털 치료제에 대한 허가를 획득한 직후 6100만달러(약 714억원) 규모 두 번째 투자(시리즈B) 유치에 성공했다. 워봇헬스(Woebot
Health)는 혁신치료제 지정을 받은 후 시리즈B를 통해 9000만달러(약 1053억원)를 투자받았다. 스윙테라퓨틱스는 자사의 근육통 관리 디지털치료제 후보가 지난 11일 FDA로부터 혁신치료제 지정받은 날 900만달러(약 105억원) 규모 시드 투자를 모금했다.
출처: news1

